Nous expliquons ce qu’est la séparation des mélanges et les méthodes qu’elle utilise. De plus, quelles sont ses caractéristiques générales et les types de mélanges.

Qu’est-ce que la séparation des mélanges ?
La séparation de mélanges ou séparation de phases est un processus physique par lequel les composants d’un mélange peuvent être séparés . Ces composants ne changent pas pendant le processus de séparation, mais restent les mêmes, seulement après la séparation, les composants ont été séparés.
Objectifs de la séparation des mélanges

Les séparations des mélanges ont différents buts ou objectifs :
- Utiliser les composants d’un mélange (homogène ou hétérogène) individuellement dans d’autres procédés.
- Quantifier séparément les substances qui les composent.
- Réaliser des combinaisons des différentes méthodes de séparation pour améliorer ou faciliter la séparation de mélanges complexes ou difficiles à séparer.
Phases d’un mélange

Il y a au moins deux phases qui composent les mélanges :
- Phase dispersée . C’est la phase qui se retrouve en moindre proportion dans le mélange. Il peut être composé d’une ou plusieurs substances dispersées ou dissoutes dans une autre (phase dispersante). Par exemple, dans une solution de sel dans l’eau, le sel est la phase dispersée ou dissoute, tandis que l’eau est la phase dispersante.
- Phase de dispersion . C’est la phase qui se retrouve en plus grande proportion dans le mélange. Une ou plusieurs phases peuvent y être dispersées ou dissoutes (phase dispersée). Dans l’exemple précédent, la phase dispersante serait de l’eau, car elle est en plus grande proportion et contient la phase dispersée ( sel ).
Types de mélanges
Il existe deux types de mélanges :
- Mélanges homogènes . Ils sont caractérisés car il n’est pas possible de distinguer leurs phases à l’œil nu (même au microscope ). Les plus courants sont les mélanges de solides avec des solides ou de liquides dans des liquides . Par exemple : eau de Javel (qui peut contenir différentes quantités de chlore), café au lait, sucre dans l’eau , limonade, teinture d’iode, entre autres. Ils sont connus sous le nom de solutions.
- mélanges hétérogènes . Ces mélanges présentent des discontinuités, c’est-à-dire que leurs différentes phases peuvent être distinguées. Quelques exemples de mélanges hétérogènes sont le ciment, l’eau de mer , le sable dans l’eau, l’eau et l’huile, l’huile et le vinaigre. À leur tour, ils peuvent être divisés en:
- Mélanges simples ou épais . Les composants peuvent être distingués ou différenciés à l’œil nu. Par exemple, une salade de laitue et de tomates.
- suspensions . Les particules de substances solides sont minuscules et il n’est pas possible de les reconnaître à l’œil nu, mais lorsque le mélange est au repos pendant un certain temps, il est possible de les distinguer au fond du récipient, au fur et à mesure qu’elles descendent à travers le liquide. Par exemple, un mélange d’eau et de talc.
Exemples de mélanges dans la vie de tous les jours
Dans nos vies, nous sommes continuellement en contact avec différents mélanges, qu’ils soient homogènes ou hétérogènes. Par exemple:
- L’eau de mer est un mélange de chlorure de sodium (NaCl), d’eau et d’autres composants.
- Le béton ou béton, utilisé dans la construction, est un mélange de ciment, d’eau, de sable et de gravier.
- Un café au lait, l’aliment de base du petit-déjeuner de la plupart des gens, est un mélange.
- Le bronze est un mélange de cuivre et d’étain appelé alliage.
Différence entre mélange et réaction chimique

Un mélange est la combinaison de deux ou plusieurs substances , mais cette combinaison n’implique pas la formation d’une ou plusieurs nouvelles substances, comme cela se produit dans une réaction chimique. Dans un mélange, les substances mélangées conservent leurs propriétés chimiques et leur composition chimique sans aucun changement.
D’autre part, dans une réaction chimique, les substances qui réagissent peuvent rompre leurs liaisons chimiques pour se recombiner d’une autre manière avec d’autres substances (qui ont également rompu leurs liaisons) et former ainsi de nouvelles liaisons, ce qui implique la formation de nouveaux composés chimiques.
Différence entre mélange et composé chimique
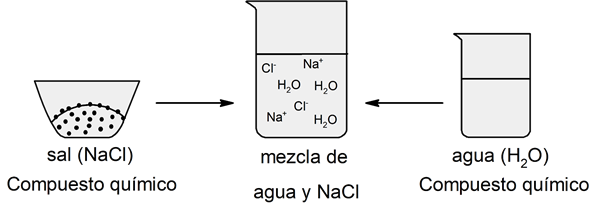
Les composants d’un mélange peuvent être séparés par des méthodes de séparation physique , tandis que les éléments qui composent un composé chimique ne peuvent pas être séparés par ces méthodes : pour cela, des méthodes de séparation chimique sont nécessaires.
La raison en est que dans les mélanges, les composants ne forment pas de liaisons chimiques, tandis que les éléments forment des liaisons chimiques pour former un certain composé chimique. De plus, dans les composés chimiques, ces éléments sont liés dans des proportions définies, ce qui permet de les représenter par des formules chimiques, alors que les mélanges ne peuvent pas être représentés de cette manière.
Propriétés physiques des mélanges
Les propriétés physiques des mélanges, telles que le point d’ ébullition ou le point de congélation , peuvent être différentes de celles de leurs composants individuels.
Par exemple, lorsque du sel de table est ajouté à l’eau (lorsqu’elle contient cette substance dissoute), le point d’ébullition du mélange augmente et le point de congélation diminue, par rapport à ceux de l’eau pure. Le premier est appelé grossissement ébulloscopique et le second décroissance cryoscopique.
Quelques méthodes de séparation des mélanges
Les méthodes de séparation de mélange sont des méthodes physiques basées sur certaines propriétés physiques des composants du mélange à séparer, telles que le point de fusion, le point d’ébullition, l’état d’agrégation, le magnétisme, etc. autres.
- Filtration . Il est utilisé pour séparer un solide d’un liquide, à condition que le solide soit insoluble dans le liquide. Un filtre est utilisé à travers lequel le mélange est passé, le solide est retenu dans le filtre et le liquide le traverse.

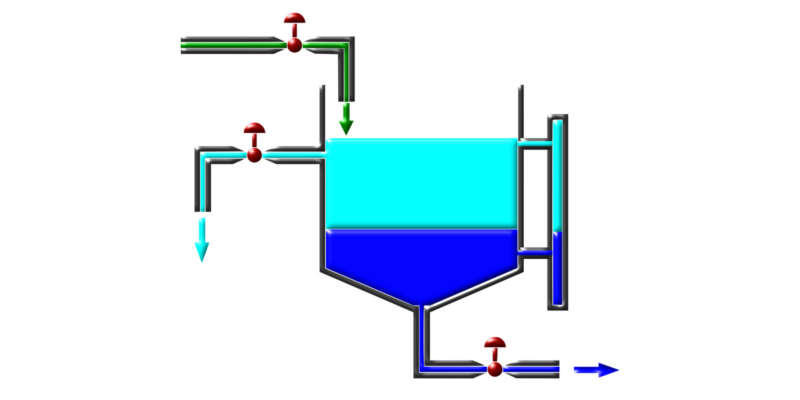
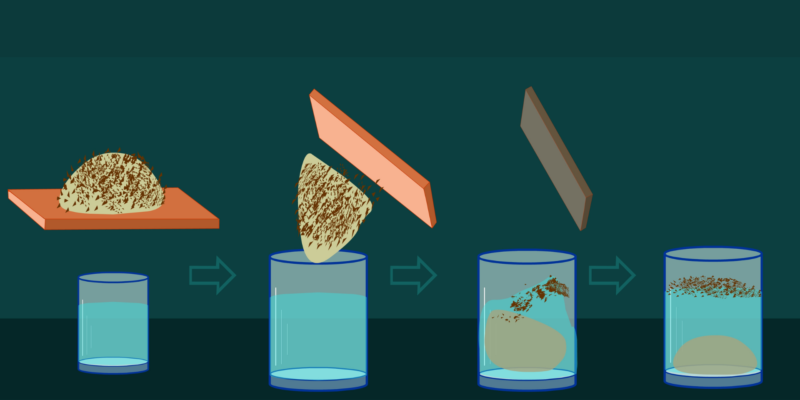
- Décantation. Il est utilisé pour séparer des mélanges de deux liquides insolubles l’un dans l’autre ou des mélanges d’un solide et d’un liquide également insolubles l’un dans l’autre. Pour réaliser la séparation, le mélange est laissé reposer dans une ampoule à décanter, la substance la plus dense descendra, tandis que la moins dense restera en surface. La clé de l’entonnoir est ensuite ouverte et la substance la plus dense peut passer.
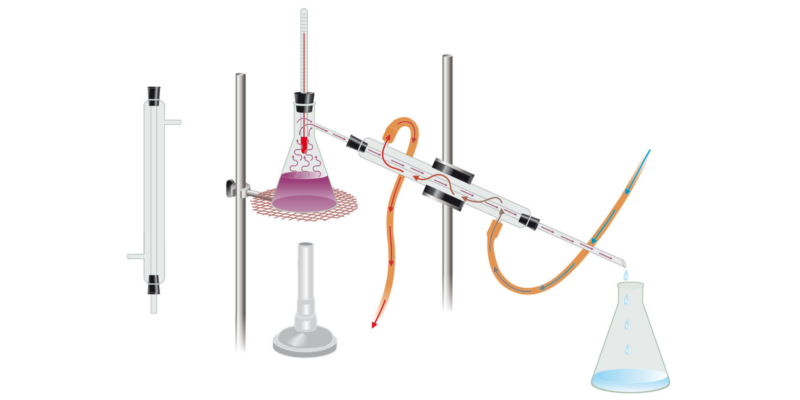
- distillation . Cette méthode est utilisée pour séparer des mélanges de liquides solubles les uns dans les autres. Il est basé sur les différences de points d’ébullition de différents liquides. Pour séparer le mélange, on lui applique d’abord de la chaleur jusqu’à ce que le liquide à bas point d’ébullition passe à la phase vapeur et qu’il se condense dans un autre récipient. De cette façon, il est séparé du liquide à point d’ébullition plus élevé, qui ne reste que dans le récipient où se trouvait le mélange à l’origine.
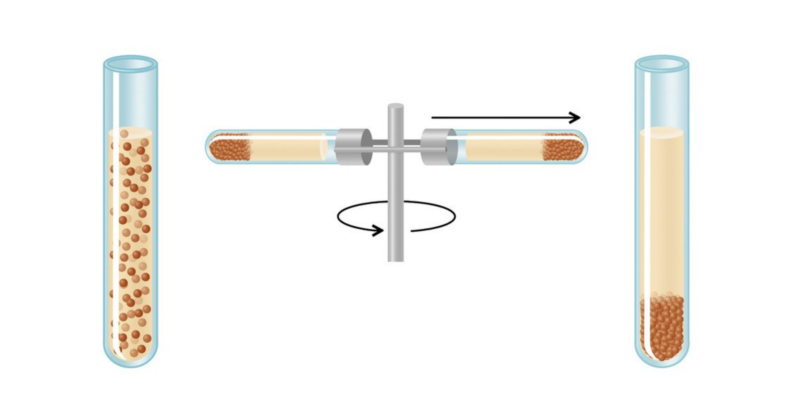
- Centrifugation . Il est généralement utilisé pour séparer un solide insoluble d’un liquide. Le mélange est centrifugé dans une centrifugeuse (un bol tournant), ce qui fait que la force centrifuge envoie le solide au fond du bol, laissant le liquide au sommet. Ils peuvent ensuite être séparés par décantation.
- Lévigation . Il est utilisé pour séparer des mélanges de solides. Les solides sont broyés et un solvant est ajouté. Ensuite, ce nouveau mélange peut être séparé selon les différentes densités de ses composants.
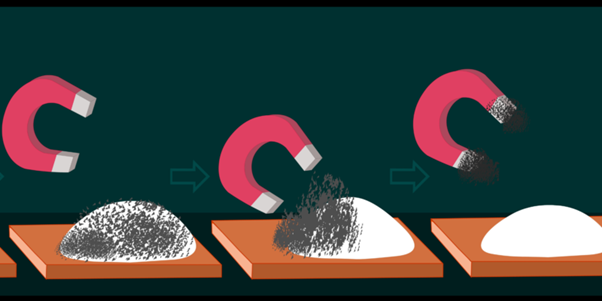
- magnétisation _ Elle consiste à séparer un mélange de substances dont au moins l’une d’entre elles possède des propriétés magnétiques et peut être attirée par un aimant.
- Lixiviation sélective . C’est une méthode qui utilise différents solvants pour séparer un mélange. Chaque composant du mélange aura plus d’affinité pour un solvant spécifique, donc lorsque chaque solvant est mis en contact avec le mélange, le composant avec la plus grande affinité pour lui se séparera. Ce procédé est largement utilisé dans les mines pour extraire l’or .

Cela peut vous aider : Colloïdes







